|
昨年のASCOで、Saltz博士は、イリノテカンに抵抗性の上皮成長因子受容体(EGFr)陽性大腸癌患者におけるモノクローナル抗体であるcertuximabと高用量のイリノテカンとの併用療法について報告した。この併用療法は、かなり良い有効率を示した。本日Saltz博士は、イリノテカン抵抗性の患者に対してcertuximab単独療法の最新のデータを報告した。
前臨床試験では、大腸癌細胞を移植した動物でcertuximabと高用量のイリノテカンとの併用療法を行い腫瘍縮小効果が得られた。Certuximab単剤療法は併用群に比べるとやや劣るものの、コントロール群に比して強い抗腫瘍効果を示した。これに引き続きcertuximabとイリノテカンの併用療法が臨床第II相試験で行われた。
Certuximabの次なる目標は単剤での抗腫瘍効果の評価であった。イリノテカン治療にもかかわらず病気の進行した転移性大腸癌患者を対象に臨床試験が行われた。全症例で腫瘍細胞にEGFrが表出されていることが確認されている。
対象患者は、performance statusが良く腎機能、肝機能、骨髄機能が保たれていることが必要であった。140の腫瘍組織標本を検索し、105個(75%)のサンプルがEGFr陽性であった。この値は上述の併用療法におけるEGFr陽性率72%と同等であり、検査の信頼度は高い。
通常の前投薬としてジフェンヒドラミンが用いられ、テスト用量のcertuximabが第1日目に投与され、翌日に400mg/m2が投与され、以後は250mg/m2が毎週投与された。57人の患者がこの治療を受けた。
57例中6例(10.5%)で有効性が認められ、21例(36.8%)でstable diseaseかminor responseが得られた。観察期間の中央値231日で、奏効期間や生存期間は中央値に達していないが、増悪期間の中央値は50日(14〜211日)であった。
|
Investigator-Adjudicated Responses
(観察期間の中央値は231日、生存期間は中央値に達していない)
- | 例数(n=57) | % | Partial
response | 6
| 10.5% | Stable
disease | 21 | 36.8% | Overall
| 27 |
47.3% |
|
アレルギー反応は3例で認められ、2例はgrade3-4であった。好中球減少や血小板減少の報告はなかった。その他の副作用は下痢(25%)、嘔気・嘔吐(46%、うち4%がgrade3-4)であった。
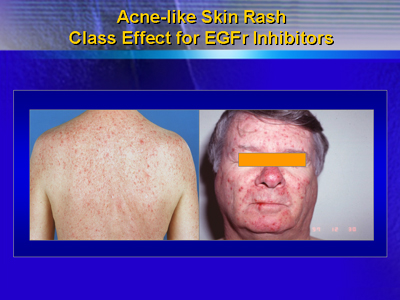
最も高率の毒性はアクネ様皮疹である。この皮疹はEGFrの阻害によるものである。皮疹は86%(うち18%がgrade3-4)に認められたが、この皮疹に対する標準的な治療はなく、抗生剤の外用薬を処方した医師もいた。
本研究では、certuximab単独で化学療法抵抗性の大腸癌に有効性が証明された。腫瘍の奏効率はイリノテカンとの併用療法が優っているが、certuximab単独投与は、毒性のプロフィールが優れており、多くの患者で治療が可能である。
|
レポーター:
Andrew Bowser | | 日本語翻訳・監修: | 東京慈恵会医科大学内科学(血液・腫瘍)助教授
東京慈恵会医科大学附属病院血液腫瘍内科診療部長
薄井紀子
|
|